Propriedades dos Estados Físicos da Matéria
Aula 1
Gases
Gases
Olá, estudante! Nesta videoaula você irá conhecer as características e propriedades dos gases. Além disso, você deverá conhecer detalhes das relações entre pressão, volume, temperatura e número de mols de um gás. Esses conteúdos são importantes para a sua prática profissional, pois são essenciais para compreender o comportamento gasoso em diversas condições. Leis como Boyle, Charles e dos Gases Ideais estabelecem relações entre pressão, volume, temperatura e quantidade de matéria, fundamentais para aplicações em química, física, engenharia e meteorologia. Esteja pronto para embarcar nesta jornada de aprendizado! Vamos lá!
Ponto de Partida
Caro estudante! Você já levou uma bola inflada em um voo e observou o que acontece? Ou já viu o funcionamento de um airbag? Ou ainda um balão de ar quente em pleno ar? Para compreender estes três acontecimentos você precisa entender um pouco sobre as propriedades dos gases e como eles se comportam em diferentes temperaturas, volumes e pressões. O ar que respiramos são gases, a água se torna gás com facilidade e a nossa atmosfera é composta por gases, então, literalmente, os gases estão por todos os lados. Mais simples que líquidos e sólidos, o estudo de gases é bastante compreendido e importante. Deste modo, nesta aula você compreenderá as leis de regem o comportamento dos gases, sejam eles considerados reais ou ideais, além disso, você conhecerá os principais processos relacionados ao comportamento dos gases, como a compressibilidade, a expansão e a efusão.
Pensando nisso, temos como ponto de partido o acionamento de um airbag durante um choque veicular. Ao haver o choque de um carro em um muro, o airbag é acionado e o motorista sofrerá menos danos. O funcionamento de airbags é bem conhecido e envolve a reação de decomposição de azida de sódio promovida pelo choque da batida. Nesta reação, são produzidos sódio e gás nitrogênio que inflam o airbag. A reação do airbag é:
Você está trabalhando em uma empresa que produz airbags para diversos compradores. Um deles solicitou um airbag para um veículo em teste, que inflado ficasse com um volume de . O comprador solicitou que a pressão dentro do airbag fosse de . Você deve, a partir das especificações do cliente, calcular quanto dos reagentes deve ser utilizado.
Então, desperte a paixão pelo conhecimento, pois em cada linha há uma revelação e em cada teoria uma oportunidade de expandir os horizontes do saber. Bons estudos!
Vamos Começar!
Caro estudante, para iniciar seus estudos sobre os gases, você precisa lembrar o conceito de pressão. A pressão é a relação entre a força exercida e a área em que se exerce esta força (Pressão = força/área). Para a atmosfera, costumamos medir a pressão utilizando um barômetro (Figura 3.1 A), em que medimos a força exercida pela atmosfera através da altura da coluna de mercúrio. Quanto maior a pressão da atmosfera, maior esta coluna. Manômetros em forma de U são bastante utilizados para medir a pressão de gases, que consistem em tubos de vidro em U preenchidos com mercúrio. O lado fechado está sob vácuo (não há nenhum gás exercendo pressão) e o outro lado está em contato com o gás que queremos saber a pressão (Figura 3.1 B).
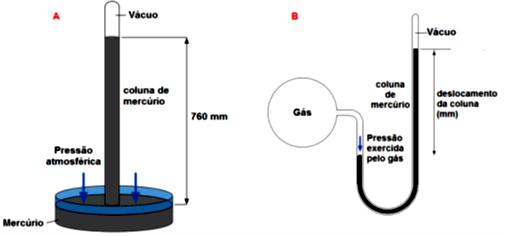
Assim como gases apresentam a propriedade de expansibilidade (ocupam todo volume disponível), eles também possuem uma propriedade chamada compressibilidade. Você evidencia isso ao apertar uma bola, ao exercer uma força na bola e ela diminui de volume, mantendo as moléculas de gás que havia no início do processo. Isso consiste em dizer que a uma determinada temperatura, o volume e a pressão de um gás são inversamente proporcionais, ou seja, quanto maior a pressão, menor o volume. Robert Boyle (1627-1691) observou esta relação, e como todos os gases apresentam este mesmo comportamento, esta relação é chamada de Lei de Boyle. A pressão e o volume se relacionam com uma constante de proporcionalidade, chamada constante de Boyle ().
Lei de Boyle: “Para uma determinada quantia de gás () a uma temperatura fixa (), o volume do gás diminui se a pressão aumenta. Por outro lado, se a pressão diminui, o volume do gás aumenta” (KOTZ, 2014, p. 484).
A partir desta lei, isolando a constante, podemos concluir que se a pressão e o volume de um gás de quantia , a uma temperatura conhecida, um segundo conjunto de condições também será: .
Você já encheu um balão e o colocou em uma câmara fria? Ou saiu de um ambiente frio com um balão murcho para um ambiente quente? A observação que relaciona volume e temperatura (em Kelvin) foi feita por Jacques Charles (1746-1823) e, como todos os gases apresentam este comportamento, ficou conhecida como a Lei de Charles (KOTZ, 2014). A temperatura e o volume se relacionam por uma constante de proporcionalidade, conhecida como constante de Charles ().
Lei de Charles: para uma determinada quantia de gás (n) a uma pressão fixa (P), o volume do gás diminui se a temperatura diminui. Se a temperatura aumenta, o volume do gás também irá aumentar.
Usando a mesma analogia apresentada anteriormente, podemos dizer que, com uma quantia e pressão constantes, o volume e a temperatura de uma condição inicial estão relacionados com o volume e a temperatura de uma condição final: .
Ao combinarmos estas duas leis, teremos a Lei Geral dos Gases. Ela permite estudarmos um gás quando os três parâmetros variam: pressão, volume e temperatura.
Outra relação que pode ser feita utilizando gases é sobre o volume e a quantidade de gás, mais precisamente sobre a quantidade de mols de um gás. Esta é a hipótese de Avogadro, observada pela primeira vez por Amadeo Avogadro (1776-1856), em 1811.
Hipótese de Avogadro: “volumes iguais de gases sob as mesmas condições de temperatura e pressão possuem iguais números de partículas” (KOTZ, 2014, p. 489).
A combinação das três leis (temperatura constante), (pressão constante) e (temperatura e pressão constantes) dá como resultado . Ao utilizarmos uma constante de proporcionalidade , teremos a Lei dos gases ideais , ou . Esta constante é universal, chamada de constante dos gases, e pode ser calculada sabendo que nas CNTP ( e ), de gás ocupa , pelo cálculo, a constante será .
Utilizando a Lei universal dos gases ideais, com três parâmetros, podemos calcular o quarto, utilizando a pressão, o volume e a temperatura para encontrar a quantidade de mols em uma amostra. Sabendo o número de mols de um gás e sua massa molar (), podemos obter a massa de composto (), calculando, assim, sua densidade. Temos, então, , com densidade , .
Você parou para pensar, que, outra característica dos gases é que eles se misturam muito bem e que, por isso, nem todo gás se encontra puro? Como o gás atmosférico que, limpo, é uma mistura de diversos gases, sendo oxigênio, nitrogênio e argônio seus principais componentes? Como você pensaria uma mistura de gases com relação à Lei universal dos gases ideais? John Dalton (1766-1844) foi o primeiro a realizar observações sobre as pressões dos gases em uma mistura, elaborando a Lei das pressões parciais.
Siga em Frente...
Lei de Dalton das pressões parciais: a pressão de uma mistura de gases é dada pela soma das pressões de cada um dos gases 1, 2, 3, ...
Em uma mistura de gases, o comportamento de cada um dos gases componentes desta mistura independe dos outros componentes. Assim como temos a pressão total sendo a soma das pressões parciais, também temos que o número total de mols é a soma do número de mols de cada um dos componentes (). Desta forma, podemos obter a Lei dos gases ideias para cada um dos componentes, ou de uma maneira total, já que para todos os gases da mistura, o volume e a temperatura são iguais:
A fração molar X de um composto (número de mols de um determinado composto dividido pelo número total de mols de todas as substâncias presentes) é uma ferramenta útil para encontrar a pressão parcial de cada um dos componentes:
Você viu até agora propriedades macroscópicas dos gases, como volume, temperatura e pressão, mas não podemos esquecer que estamos falando de moléculas e que o comportamento microscópico resulta nas propriedades que vimos. Analisar os gases, observando seus átomos, consiste na Teoria Cinético-Molecular dos Gases, e, para isso, você precisa ter algumas considerações:
- Gases são constituídos de partículas (moléculas ou átomos) em grande número e sempre em movimento.
- As partículas de um gás são pequenas e a distância entre elas é maior que seu tamanho.
- O movimento destas partículas ocorre em linha reta, exceto quando as moléculas se chocam umas com as outras ou com as paredes dos recipientes. Quando isso ocorre, a energia cinética é conservada. E esta é a única interação entre estas partículas.
- A energia cinética média de todas as partículas de um gás é igual para todas as partículas de um gás, independentemente da massa molecular, sendo proporcional à temperatura deste gás.
Você pode perceber que as partículas de um gás estão em movimento quando, por exemplo, sente o perfume de alguém que acabou de entrar em uma grande sala. O aroma que seu olfato detecta são moléculas que se tornaram gasosas e se moveram pelo ar. O movimento de moléculas de gás ocorre em diferentes velocidades e em uma determinada temperatura a maioria das moléculas percorre uma velocidade intermediária, algumas poucas uma velocidade menor e outras uma velocidade maior, sendo que a velocidade das moléculas de um gás pode ser descrita como apresentando uma distribuição normal. A velocidade das moléculas de um gás está relacionada com a temperatura e o tamanho das moléculas do gás.
Para avaliarmos a relação entre a velocidade e a temperatura, precisamos pensar em como calcular a energia cinética. Para uma molécula de massa , a energia cinética () é dada por:
Como as moléculas de um gás apresentam velocidades diferentes, não é possível calcular a energia cinética para todo o gás, mas podemos calcular a energia cinética média, utilizando a velocidade média:
Experimentalmente, a energia cinética média de um gás corresponde à temperatura vezes 3/2 de R: Portanto, quanto maior a temperatura, maior a energia cinética, o que significa que maior será a velocidade das moléculas. Com relação à massa, você espera que moléculas menores se movam com mais facilidade.
Os gases se misturam com facilidade. Você pode racionalizar este fenômeno pensando no movimento aleatório das moléculas de todos os gases. O movimento natural dos gases é chamado difusão. Se você colocar dois ou mais gases em uma câmara fechada sem nenhuma interferência externa, mesmo assim, após um determinado tempo, os gases estarão completamente misturados devido a este movimento molecular.
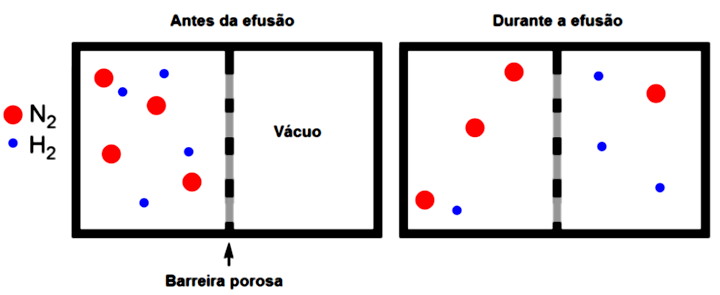
Outro movimento dos gases é a efusão, conforme apresentado na Figura 3.2, que consiste na passagem destes gases por uma minúscula abertura em um recipiente com pressão muito baixa. O movimento de gases ocorre com maior velocidade inversamente proporcional à sua massa molecular, portanto, a taxa em que um gás se move de um lugar para outro deve ter a mesma relação. Thomas Grahn (1805-1869) determinou esta taxa como sendo a taxa de efusão e observou que ela é inversamente proporcional à raiz quadrada da massa molar do gás. Com isso, podemos comparar a taxa de efusão de dois gases pela Lei de Graham.
A Lei dos gases ideais é completamente aplicável para gases próximos à temperatura ambiente, com uma pressão de . Em outras condições ocorrem alguns desvios na relação , isso devido à suposição de que moléculas de gás possuem volumes desprezíveis e de que não há nenhum tipo de força entre elas.
Pressões muito elevadas fazem com que o espaço disponível para o movimento das moléculas seja menor. Embora com volume pequeno, nas suposições realizadas nesta aula, em nenhum momento se levou em conta que as moléculas ocupam uma parte do volume disponível para o movimento. Porém, se elevarmos muito a pressão, mais o volume da molécula influencia no volume do gás e na temperatura, levando a alterações na Lei dos gases ideais.
Moléculas próximas apresentam determinadas interações, chamadas de interações intermoleculares. Se considerarmos que este tipo de interação também ocorre com as moléculas de gases ao se chocarem, teremos uma variação na energia cinética, sendo que até agora consideramos que não ocorria nenhuma variação. Quanto mais baixa a temperatura, mais este tipo de interação é observado e maior será o desvio da lei dos gases ideais.
Vamos Exercitar?
Estudante, a matéria pode ser encontrada majoritariamente nos estados sólido, líquido ou gasoso. Desse modo, é preciso compreender as características, propriedades e comportamento da matéria no estado que ela se encontra. O estado gasoso é caracterizado pela matéria que não possui nem forma e nem volume definido. A compreensão da matéria em estado gasoso permite o desenvolvimento de processos industriais, como a produção de gases industriais e a síntese de compostos químicos, além de ser crucial na modelagem de fenômenos atmosféricos e no projeto de sistemas de ventilação e purificação de ar. Desse modo, é importante conhecer as leis que regem o comportamento dos gases nos diferentes estados físicos da matéria.
Assim, vamos resolver este problema da azida proposto inicialmente, você deve utilizar os conceitos estequiométricos, partindo dos dados do gás, obtendo quantos mols de gás nitrogênio devem ser obtidos, e utilizando os fatores estequiométricos descobrir quantos mols de azida de sódio devem ser utilizados.
Sobre o gás, usaremos , sendo que você deve considerar a temperatura ambiente de ) e a pressão para ):
de gás nitrogênio.
Se de formam de , para formar de gás, deve reagir de azida de sódio. Como a massa molar da azida de sódio é , correspondem a de reagente.
Utilizando esta quantia, em um saco de airbag de , ao ocorrer o choque e, em decorrência, a decomposição da azida, será formado gás suficiente para que o airbag tenha uma pressão de .
Você pode pensar em pontos extras e adicionais sobre o problema apresentado. Continue estudando!
Saiba Mais
Para saber mais sobre o conceito de gases, acesse a biblioteca virtual e faça a leitura do capítulo 10, Gases, do livro “Química: a ciência central, disponível na biblioteca virtual [Biblioteca Virtual 3.0].
BROWN, T. L. et al. Química: a ciência central. 1. ed. São Paulo, SP: Pearson, 2016. E-book. Disponível em: https://plataforma.bvirtual.com.br. Acesso em: 05 fev. 2024.
Para compreender e aprofundar seus conhecimentos sobre gases reais e ideais, faça a leitura do texto: “Gases Ideais e Reais”, disponível em: <https://cesad.ufs.br/ORBI/public/uploadCatalago/18473316022012Quimica_I_Aula_9.pdf>. Acesso em: 21 fev. 2024.
Por fim, você pode aprender mais sobre as leis dos gases ideais por meio da leitura do artigo “Lei dos Gases Ideais”, disponível em: <http://doi.org/10.24927/rce2015.095>. Acesso em: 21 fev. 2024.
Referências Bibliográficas
DREKENER, R. L. Química Geral. Londrina: Editora e Distribuidora S.A., 2017
KOTZ, J. C. et al. Química geral e reações químicas.2. ed. v. 1. São Paulo: Cengage Learning, 2014.
Aula 2
Líquidos
Líquidos
Olá, estudante! Nesta videoaula você irá conhecer as características e as propriedades das substâncias que se encontram em estado líquido, assim como as forças intermoleculares. Esse conteúdo é importante para a sua prática profissional, pois as substâncias líquidas desempenham um papel crucial em várias indústrias, como química e farmacêutica. Suas propriedades físicas e químicas são fundamentais para processos de produção e formulação e as forças intermoleculares afetam suas características e comportamento, influenciando suas aplicações. Preparado para embarcar nessa jornada de aprendizado? Vamos lá, então!
Ponto de Partida
Olá, estudante! Devido à distância entre as moléculas de um gás, consideramos que, em uma situação ideal, a interação entre as moléculas é nula, então, as propriedades independem da natureza do gás, ou seja, as moléculas que o compõem. Nos líquidos isso já não ocorre, as moléculas estão bem mais próximas que nos gases e passamos a ter que entender estas interações.
Nesta aula você irá conhecer e compreender as propriedades e as características das substâncias que se encontram em estado líquido. Além disso, conhecerá e compreenderá as características das ligações secundárias, conhecidas também como forças intermoleculares.
Pensando nestes pontos, você se colocará no lugar de um trabalhando no setor de pesquisa e desenvolvimento de uma indústria farmacêutica. Você ficou encarregado de realizar experimentos sobre a lipofilicidade de moléculas candidatas a fármacos e elaborar um relatório selecionando as moléculas mais proeminentes. A membrana celular é composta por lipídios, que são moléculas de cadeia carbônica longa, contendo em uma das extremidades, um grupo polar. A lipofilicidade de uma molécula mede a sua solubilidade ao passar pela barreira lipídica. Com os conhecimentos adquiridos você deverá compreender e aplicar o método para calcular a lipofilicidade de moléculas de interesse. Bons estudos e vamos em frente!
Vamos Começar!
Estudante, os gases são facilmente descritos devido à distância entre as moléculas ser relativamente grande. Devido a esta distância, eles apresentam uma característica que os líquidos e sólidos não apresentam: a compressibilidade. Ao aplicarmos uma pressão, os gases são comprimidos, já os líquidos e os sólidos resistem a esta força, apresentando uma falta de compressibilidade. A aproximação existente entre as moléculas torna a descrição de sólidos e líquidos mais complexa que para gases.
Mas o que define o estado em que a matéria se encontra a uma determinada temperatura? Se analisarmos a temperatura ambiente, algumas moléculas são sólidas, como o , outras são líquidas, como a água, e outras são gases, como o oxigênio. As fases da matéria englobam os três estados físicos: sólido, gasoso e líquido, sendo que as moléculas assumem os três estados, dependendo das condições de temperatura e pressão. A fase que a molécula adota em uma determinada condição está relacionada com a proximidade entre as moléculas, sua energia cinética e as forças intermoleculares. Veremos mais adiante que moléculas que apresentam uma forte atração entre si, como a água, precisam estar a para passar para o estado líquido e para o gasoso. Agora, ao analisarmos o gás cloro (), ele passa de sólido para líquido a uma temperatura de e de líquido para gás a , sendo um gás nas CNTP.
Em um gás, a força atrativa entre as moléculas é menor que a energia cinética, não permitindo que elas fiquem próximas, enquanto em líquidos e sólidos esta atração supera a energia cinética, mantendo as moléculas próximas. Dos três estados, o líquido é o mais difícil de ser descrito, pois as moléculas não são completamente independentes, como nos gases ideais, e nem tão próximas, como nos sólidos. Os elementos se conectam por ligações químicas iônicas, covalentes ou metálicas, sempre atingindo a regra do octeto. Porém, além destas interações consideradas fortes, que mantêm as moléculas formadas, existem forças entre moléculas próximas que não são tão intensas quanto uma ligação, as chamadas interações ou forças intermoleculares. Estas forças são responsáveis pela solubilidade de um composto em outro (em qualquer um dos estados), ou ainda pela forma que as moléculas adotam, como o DNA que existe como uma dupla hélice. Além disso, são responsáveis por diversas propriedades dos líquidos.
A dualidade entre as forças intermoleculares e a liberdade de movimento das moléculas leva a propriedades interessantes. A viscosidade é uma delas, que consiste na resistência de um líquido ao escoamento. Quanto maior for a viscosidade, mais lento um líquido escoa. Esta propriedade é causada pelas interações entre as moléculas do líquido, sendo que você pode raciocinar que quanto mais intensa as forças intermoleculares, maior a viscosidade, pois haverá menos liberdade de movimento entre as moléculas. Além das forças intermoleculares, para hidrocarbonetos de cadeias longas, o entrelaçamento destas cadeias dificulta o escoamento. Normalmente, o aumento da temperatura, resulta em menor viscosidade. Isso ocorre devido à energia das moléculas aumentar com o aumento da temperatura, levando a uma maior movimentação molecular, facilitando o escoamento.
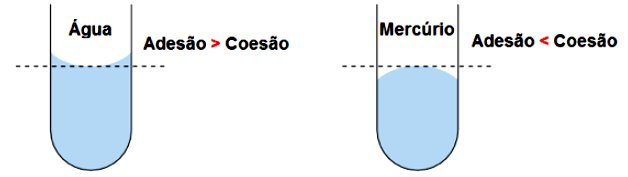
A interação entre as moléculas dentro de um líquido faz com que elas se mantenham juntas, conduzindo-as para o centro do líquido. Esta característica é definida como tensão superficial, que define a superfície de um líquido e faz, por exemplo, que líquidos com interações intermoleculares fortes formem esferas (a gota é resultado da ação da gravidade). O esperado é que líquidos com interações intermoleculares mais fortes apresentem maior tensão superficial. Na literatura, você consegue encontrar diversos valores de tensão superficial tabelados (ATKINS; JONES, 2012, p. 180). Assim como a viscosidade, pelo mesmo efeito, o aumento da temperatura leva a uma diminuição da tensão superficial. Se você colocar um líquido em um tubo estreito, ele irá se elevar neste tubo. Isto ocorre devido à ação capilar, que nada mais é que a interação entre as moléculas do líquido com as moléculas da parede do tubo. Esta força é chamada de adesão, definida como forças que ocorrem entre as moléculas do líquido e da superfície, mantendo-as juntas. As interações que ocorrem entre moléculas de um mesmo material (líquido-líquido ou superfície-superfície) são chamadas de forças de coesão. A diferença entre estas forças leva à formação de meniscos (superfícies curvas) nos líquidos nestes tubos. Quando as forças de adesão se sobrepõem às forças de coesão, há a formação de um menisco côncavo, como na água em um tubo de vidro. Agora, quando as forças de coesão são mais fortes que as forças de adesão, há a formação de meniscos convexos, como o mercúrio em um tubo de vidro. Você pode observar os dois casos na Figura 3.3.
Como mencionado, em um líquido, quanto mais temperatura fornecemos, maior é a energia cinética das moléculas deste líquido. Quando as moléculas possuem energia cinética o bastante para escapar das interações com as moléculas vizinhas, elas passam do estado líquido para o estado gasoso. Esse processo é chamado de vaporização (ou evaporação), ou seja, para que uma substância passe do estado líquido para o gasoso, é preciso adicionar calor (esta variação de energia é conhecida como entalpia molar de vaporização padrão, ).
Na vaporização, como estamos fornecendo energia ao sistema, o valor da entalpia é positivo, temos um processo endotérmico. Quanto maior forem as atrações entre as moléculas, maior deve ser a entalpia molar de vaporização, ou seja, mais energia deve ser fornecida ao sistema para que passe para a fase gasosa. O processo inverso da vaporização é a condensação, sendo este um processo exotérmico, ou seja, libera calor para o meio.
O que acontece se você coloca água em um béquer e o sela? Inicialmente, mesmo sem estar aquecendo, um pouco de água irá evaporar, até que nada mais seja observado a olho nu. Neste ponto, a taxa de evaporação é igual à taxa de condensação, ou seja, a quantidade de água que evapora é igual à quantidade de água que. Você não observa nenhuma mudança macroscópica porque a velocidade das moléculas que passam do líquido para vapor é igual à velocidade das moléculas que passam do vapor para o líquido. Em um sistema fechado como o béquer, após atingir o equilíbrio, a pressão que o vapor exerce sobre o líquido é denominada pressão de vapor de equilíbrio. Se você pensar que quanto mais vapor tivermos, maior será a pressão exercida, a pressão de vapor nos diz a tendência que as moléculas têm de evaporarem, sendo quanto maior a pressão de vapor, mais volátil o composto.
Em um líquido, a energia cinética das moléculas se assemelha à distribuição de energia de gases (uma curva normal de distribuição). Portanto, quanto maior a temperatura, maior será a energia cinética média das moléculas, com isso, maior será o número de moléculas com energia suficiente para escapar da superfície do líquido. Esta relação nos diz que a pressão de vapor deve aumentar com o aumento da temperatura, até atingir a pressão atmosférica, ocorrendo neste momento a evaporação.
Siga em Frente...
A temperatura em que a pressão de vapor se iguala à pressão atmosférica é denominada de ponto de ebulição (chamado normal a ). Como a pressão atmosférica varia de acordo com a altitude, o ponto de ebulição também irá variar, sendo que, em lugares altos com pressão atmosférica maior que o nível do mar, a água irá ferver a uma temperatura menor que 100 °C, já em lugares abaixo do nível do mar, em que a pressão é maior, a água ferve a temperaturas mais baixas. No nível do mar (), o ponto de ebulição da água é exatamente (ponto de ebulição normal). Voltando ao béquer selado e ao equilíbrio entre líquido e vapor, se o abrirmos, o equilíbrio não será atingido, pois a água gasosa formada se mistura com as moléculas de ar, sendo que mais moléculas gasosas são formadas. Será que é assim que você consegue secar roupa? Até agora falamos bastante em forças intermoleculares. Para discutirmos estas interações, você precisa ter claro que à medida que moléculas se aproximam, ocorre uma força atrativa entre elas, esta força leva a uma diminuição da energia do sistema (maior estabilidade). Porém, quando esta distância se torna muito pequena, passam a ocorrer forças de repulsão, que levam a um aumento de energia potencial, ou seja, para cada tipo de interação existe uma distância mínima entre as moléculas, quando o sistema se encontra mais estável. Veremos as interações intermoleculares uma a uma:
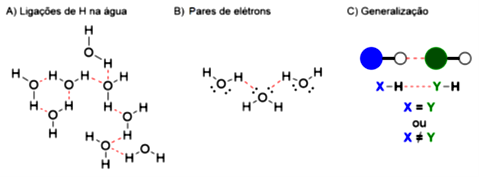
1) Ligação de hidrogênio: das forças intermoleculares, esta é a mais forte, ocorrendo apenas em moléculas que contenham as ligações . Nestas moléculas o hidrogênio está ligado a átomos bastante eletronegativos, levando a ligações fortemente polarizadas. Isso resulta em uma elevada deficiência de carga no átomo de , que assume uma carga positiva parcial, enquanto o elemento eletronegativo assume uma carga parcial negativa. Com isso, ocorre uma atração entre as cargas opostas de moléculas vizinhas, levando a uma forte interação entre elas. Por exemplo, para a água temos a Figura 3.4A, mostrando como as moléculas se ligam, em 3.4B mostramos a interação dos pares de elétrons. A ligação de hidrogênio é representada por uma ligação pontilhada para qualquer um dos três átomos eletronegativos, como desenhado na Figura 3.4C.
É esperado que moléculas semelhantes contendo átomos de um mesmo grupo apresentem um padrão de aumento do ponto de fusão e de ebulição na medida em que aumenta o tamanho molecular. Ao compararmos moléculas semelhantes do grupo do carbono (14), observamos esta tendência, sendo que o metano () apresenta o menor ponto de ebulição, enquanto apresenta o maior ponto de ebulição. Entretanto, ao compararmos moléculas do grupo do oxigênio (16), o esperado era que a água apresentasse o menor ponto de ebulição e o maior, porém a água tem o maior ponto de ebulição entre as moléculas semelhantes deste grupo. O mesmo ocorre nos grupos 15 (do nitrogênio) e 17 (do flúor). Esta observação experimental pode ser justificada pela presença de ligações de hidrogênio, já que os elementos que formam moléculas com esta alteração são os mais eletronegativos (, , ). A presença de interações intermoleculares faz com que seja necessária mais energia para separar as moléculas e elas passarem ao estado gasoso.
2) Interação íon-dipolo: quando falamos em ligações covalentes polares, você aprendeu que a diferença de eletronegatividade levava à formação de polos de cargas parciais negativa () e positiva (). Quando temos um íon na presença de uma molécula polar, ocorre uma interação entre este íon com o polo de carga oposta à sua. Cátions serão atraídos pela carga parcial negativa, enquanto ânions serão atraídos para a carga parcial positiva. Esta interação é eletrostática, portanto, quanto mais próximos estiverem o íon e o dipolo, maior será a atração, para íons com maiores cargas, a atração também será maior, valendo o mesmo para o momento de dipolo, quanto maior, maior a força atrativa, conforme apresentado na Figura 3.5. Quando estamos dissolvendo íons em água, é esta força que está em vigor. Este processo sofre uma variação de entalpia, conhecida como energia de solvatação, ou entalpia de hidratação. Quanto mais energia é liberada no processo de solvatação, maior a interação entre o íon e a molécula.
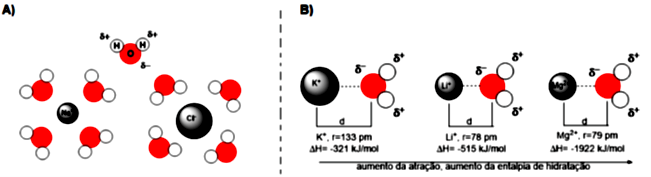
3) Interação dipolo-dipolo: em moléculas polares, quando a diferença de eletronegatividade não é tão grande como nas ligações , , , não ocorre a formação de ligações de hidrogênio, mesmo havendo polos parciais positivos e negativos. Este é o caso, por exemplo, da ligação . A formação de polos faz com que ocorra uma interação eletrostática entre as moléculas, esta interação é chamada dipolo-dipolo, podendo ser representada como na Figura 3.6.
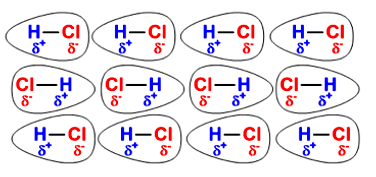
Você deve pensar que no estado sólido, as moléculas apresentam pouca liberdade de se movimentarem, sendo mais fácil que ocorra este alinhamento. Com isso, as moléculas apresentam um efeito atrativo entre si. Para os líquidos, como há uma liberdade de movimento, os polos nem sempre se encontram alinhados, ocorrendo, em alguns momentos, interações atrativas (cargas opostas próximas) e em outros, atrações repulsivas (cargas iguais próximas). Quando duas moléculas estão com os polos opostos próximos, elas se mantêm nesta posição mais tempo que quando temos polos de mesmo sinal próximos, este efeito resulta em uma força líquida atrativa, mantendo as moléculas unidas. Com relação ao ponto de ebulição, quanto maior o momento de dipolo de uma molécula (), maior será o seu ponto de ebulição, pois maior será a interação dipolo-dipolo. Para podermos realizar esta comparação, devemos utilizar moléculas de massa molar () semelhantes, como na série de moléculas: propano (, e ), éter dimetílico (, e ), cloreto de metila (, e ), acetaldeído (, e ) e acetonitrila (, e ).
4) Interação dipolo-dipolo induzido: moléculas que possuem um dipolo permanente podem induzir dipolos temporários em moléculas apolares. Isso ocorre porque a nuvem eletrônica da molécula polar, ao se aproximar da molécula apolar, induz uma alteração nesta segunda nuvem eletrônica. Isso ocorre quando temos água na presença de . Oxigênio é uma molécula apolar, pois a nuvem eletrônica está igualmente dividida entre os dois átomos de oxigênio e a água já sabemos que é polar. Ao se aproximarem, estas duas moléculas se atraem, pois o polo negativo da água induz um polo positivo na molécula de oxigênio, isto permite, por exemplo, dissolvermos oxigênio em água, conforme apresenta a Figura 3.7.
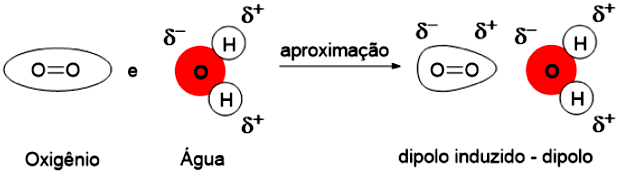
Esta indução de uma nuvem eletrônica em outra é a polarização, e quanto mais facilmente isso ocorre, mais polarizável é a molécula que tem a nuvem influenciada.
5) Interações de London (dipolo induzido-dipolo induzido): embora moléculas apolares possuam nuvens eletrônicas igualmente divididas entre os dois átomos, em determinados momentos, atrações e repulsões instantâneas entre núcleos e elétrons vizinhos fazem com que ocorram dipolos momentâneos, quando moléculas vizinhas apresentam este dipolo momentâneo induzido pela vizinhança, ocorre interação dipolo induzido-dipolo induzido, conforme apresentado na Figura 3.8. Essas interações levam à diminuição da energia do sistema, estabilizando-o.

As forças intermoleculares apresentam energias diferentes, sendo que quanto maior a energia típica, maior a sua força. A energia de uma interação eletrostática forte íon-íon apresenta energia típica de . As ligações de hidrogênio são em média 10 vezes mais fracas (cerca de ). Interações entre moléculas polares íon-dipolo e dipolo-dipolo possuem energia de e , respectivamente. Nas moléculas apolares (dipolo induzido-dipolo induzido e de London) apresentam energia típica de
(ATKINS; JONES, 2012, p. 172). As interações íon-dipolo, dipolo-dipolo, dipolo-induzido e London são conhecidas como forças de Van der Waals.
Vamos Exercitar?
Estudante, nesta aula você trabalhou com as características e as propriedades dos líquidos, conheceu algumas propriedades características das substâncias que se encontram nesse estado físico, como a capitalidade e a tensão superficial, além disso, conheceu as características das ligações secundárias, como a ligação covalente polar, a ligação de hidrogênio e as forças de Van der Waals.
Pensando no exposto, vamos retomar a situação proposta do cálculo da lipofilicidade de substâncias. As moléculas de lipídios possuem uma cadeia carbônica com vários átomos de carbono, por isso apresentam interações de London. Para determinar a lipofilicidade, você precisa avaliar a solubilidade de drogas em lipídios. Devido à sua viscosidade (entrelaçamento de cadeias longas), realizar experimentos de avaliação de solubilidade diretamente em lipídios não é muito prático. Uma alternativa é utilizar um solvente orgânico apolar, um hidrocarboneto que se aproxime das características dos lipídios, ou seja, deve apresentar o mesmo tipo de interação intermolecular com as drogas. O octano é uma excelente alternativa para isso, por ter apenas carbonos e hidrogênios em sua estrutura é uma molécula apolar, fácil de ser removida em rota-evaporador e não evapora com facilidade a temperatura ambiente ().
Para determinar a afinidade de uma molécula pelo octano, fazemos um experimento com a droga candidata e dois solventes, um apolar e outro polar. Assim, saberemos se as moléculas apresentam mais características polares ou apolares.
O coeficiente de partição () é a maneira como se determina a lipoficilidade das moléculas, sendo ele a razão entre as concentrações da droga na fase orgânica () e na fase aquosa (): .
Quanto maior o coeficiente de partição, mais solúvel a droga é em solventes apolares. Como nosso corpo é constituído majoritariamente por água, o solvente polar utilizado neste teste é a água. Então, você deve solubilizar a droga em uma mistura de água e octanol, agitar e verificar quanto da droga está em cada uma das fases, determinando a concentração nas duas fases e calculando o coeficiente de partição.
Se um fármaco é bastante lipofílico, ele entrará na célula com facilidade, saindo da corrente sanguínea. Como o interior da célula é onde ele irá apresentar sua atividade biológica, o esperado é que elevados valores de signifiquem melhores fármacos. Entretanto, isso não é uma relação tão direta, e elevados valores de , significam baixa solubilidade em água, sendo difíceis de serem administrados.
Entre as três moléculas estudadas, com atividades in vitro semelhantes, duas delas apresentaram valores de e e uma terceira um valor de . Como o estudo envolve a pesquisa por drogas de administração oral, você sinalizou como mais interessante as duas drogas com menor liposolubilidade ( e ). Para sua ciência,
é o coeficiente de partição do paracetamol (BARREIRO; FRAGA, 2008). Além disso, você pode pensar em pontos extras e adicionais sobre o problema apresentado. Continue estudando!
Saiba Mais
Para saber mais sobre as substâncias que se encontram em estado líquido, acesse a biblioteca virtual e faça a leitura do capítulo 5, Gases, líquidos e sólidos, do livro “Introdução à química geral”, disponível na Minha Biblioteca.
BETTELHEIM, Frederick A.; BROWN, William H.; CAMPBELL, Mary K.; FARRELL, Shawn O. Introdução à química geral. São Paulo: Cengage Learning Brasil, 2016. Disponível em: https://integrada.minhabiblioteca.com.br/#/books/9788522126354/. Acesso em: 25 jan. 2024.
Para compreender e aprofundar seus conhecimentos sobre as forças intermoleculares, principalmente, sobre a ligação de hidrogênio, faça a leitura do artigo: “O estado da arte da Ligação de Hidrogênio”, disponível em: https://doi.org/10.5935/0100-4042.20150146. Acesso em: 29 fev. 2024.
Por fim, aprofunde seus conhecimentos e amplie seus conhecimentos sobre as propriedades dos líquidos por meio da leitura do artigo: “Tensão superficial estática de soluções aquosas com óleos minerais e vegetais utilizados na agricultura”, disponível em: https://doi.org/10.1590/S0100-69162007000200003. Acesso em: 29 fev. 2024.
Referências Bibliográficas
ATKINS, P.; Jones, L. Princípios de química - questionando a vida moderna e o meio ambiente. 5. ed. Porto Alegre: Bookman, 2009.
BARREIRO, E. J.; FRAGA, C. A. M. Química medicinal: as bases moleculares da ação dos fármacos. 2. ed. Porto Alegre: Artmed; 2008.
KOTZ, J. C. et al. Química geral e reações químicas. 2. ed. São Paulo: Cengage Learning, 2014. v. 1.
RUSSEL, John B. Química geral. v. 2, 2. ed. São Paulo: Pearson Education do Brasil, 2011.
Aula 3
Sólidos
Sólidos
Olá, estudante! Nesta videoaula você irá conhecer os compostos em estado sólido, suas propriedades e características e os arranjos formados pelos átomos na estrutura quando apresentam arranjo cristalino. Esse conteúdo é importante para a sua prática profissional, pois são fundamentais em várias áreas profissionais, como materiais, engenharia, geologia e ciência dos materiais. Compreender esses aspectos permite o desenvolvimento de novos materiais, a otimização de processos de fabricação e a resolução de problemas em compostos sólidos. Esteja preparado para embarcar nesta jornada de aprendizado! Vamos lá!
Ponto de Partida
Olá, estudante! Nesta aula vamos explorar o fascinante mundo dos compostos sólidos e suas estruturas cristalinas. Ao estudar a estrutura de compostos cristalinos, você terá a oportunidade de mergulhar em conceitos como redes cristalinas e estruturas de Bravais, compreendendo como os átomos se organizam em arranjos tridimensionais. Além disso, ao entender a célula unitária e o empacotamento dos átomos nos sólidos, você descobrirá como esses arranjos influenciam diretamente as propriedades dos materiais, como sua densidade, condutividade elétrica e térmica, e resistência mecânica.
Adicionalmente, ao aprender sobre as aplicações de compostos sólidos, você verá como esses conceitos são essenciais em diversas áreas, desde a fabricação de materiais para eletrônicos e dispositivos médicos até o desenvolvimento de novos materiais para construção civil, transporte e indústria automotiva.
Para compreender melhor sobre esses compostos e suas características, vamos atuar na pesquisa de novos materiais sólidos. Desse modo, imagine que você foi contratado para trabalhar em uma empresa que estava entrando no ramo de pesquisa de novos materiais. Seu primeiro desafio foi selecionar qual metal pode ser utilizado em um projeto de obtenção de novas ligas com alta densidade, que deverão ser aplicadas na construção de equipamentos ultra resistentes. A ideia central desta pesquisa é encontrar um metal com fator de empacotamento atômico baixo, sinalizando que existem muitos espaços entre os átomos que poderão ser preenchidos por outros elementos. Quais metais você indica para iniciarem os testes? Bons estudos!
Vamos Começar!
Estudante, quando você reduz a temperatura até o ponto de as moléculas terem energia cinética tão baixa que não “escapam” dos seus vizinhos, você obtém um composto na sua forma sólida. Esta temperatura varia de molécula para molécula, por exemplo, a água é sólida a temperaturas abaixo de .
A natureza dos sólidos (metálicos, iônicos ou moleculares) define suas características físico-químicas. Um sólido cristalino é aquele em que os átomos, íons ou moléculas se encontram em um arranjo ordenado, já um sólido amorfo, é aquele que não apresenta nenhum tipo de organização periódica ou regular dos constituintes do sólido. As faces de um sólido cristalino são comumente planas, com ângulos bem definidos entre si. Já um sólido amorfo só apresenta uma face definida se for moldado ou cortado. Um mesmo composto pode ser encontrado como um cristal ou um sólido amorfo, dependendo do processo de obtenção, sendo estas formas conhecidas como alotrópicas. Um exemplo disso é o óxido de silício () que pode ser encontrado como o cristal quartzo ou na forma amorfa como no vidro.
Os sólidos cristalinos são classificados de acordo com o tipo de ligação que mantém a conectividade dos seus constituintes: moleculares, reticulares, metálicos ou iônicos.
1) Sólidos moleculares: moléculas covalentes que se mantêm próximas devido às interações intermoleculares. Suas características dependerão destas interações. Como elas apresentam baixa grandeza de força, sólidos moleculares apresentam pontos de fusão baixos. Para a água, a , o sólido apresenta ligações de hidrogênio, mesmo tipo de interação da sacarose. Como estas interações são fortes, as moléculas são bastante duras. Você deve notar que, apesar de apresentarem o mesmo tipo de interação intermolecular, os compostos apresentam pontos de fusão bem diferentes, sendo que a glicose se decompõe antes de fundir, a uma temperatura de . Estes sólidos podem ser cristalinos ou amorfos, e a graxa de silicone é um exemplo de sólido amorfo. Comumente, os sólidos moleculares são mais densos que os líquidos, sendo a água uma exceção, devido à formação mais rígida de ligações de hidrogênio, conforme apresentado na Figura 3.9.
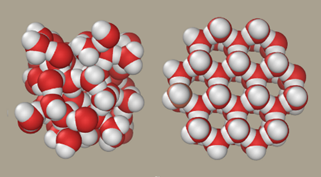
2) Sólidos reticulares: os átomos em sólidos reticulares são ligados a seus vizinhos por ligações covalentes fortes, formando uma rede que se estende ao longo do sólido e, por isso, são duros e rígidos, com elevados pontos de fusão e insolubilidade em água. Assim como o óxido de silício, o carbono também apresenta duas formas alótropas, ou seja, são o mesmo elemento que difere na maneira como os átomos se conectam. No diamante, os átomos de carbono se ligam a outros quatro átomos de carbono, enquanto na grafita, o átomo de carbono se liga a outros três átomos, em moléculas planas, conforme apresentado na Figura 3.10.

Siga em Frente...
3) Sólidos metálicos: átomos de elementos metálicos mantêm seus cátions unidos por um mar de elétrons. Sódio metálico são cátions em um mar de elétrons, caracterizando a ligação metálica. Metais são maleáveis, dúcteis, lustrosos, bons condutores térmicos e elétricos. Grande parte destas características pode ser explicada pela maneira como os cátions se organizam. Eles adotam uma estrutura de empacotamento compacta, ocorrendo o empilhamento de cátions, deixando sempre o menor espaço vazio entre estes.
A menor unidade de repetição em um sólido cristalino é chamada de cela unitária (ou célula unitária). Ela se repete ao longo do sólido metálico cristalino, sendo que o formato da célula unitária depende da relação entre os ângulos (, e ) e as arestas (, e ). A relação entre ângulos e arestas leva a 14 padrões básicos, denominados retículos de Bravais, apresentados na Figura 3.11. Quando os átomos ocupam as posições dos vértices, dizemos que o arranjo é uma cela simples ou primitiva (). Quando existe um átomo no centro da cela unitária, o arranjo é chamado de cela corpo centrado (), quando eles estão nos vértices e em cada face, é chamado de cela face centrado (), temos, ainda, uma situação em que os átomos estão em duas faces opostas.
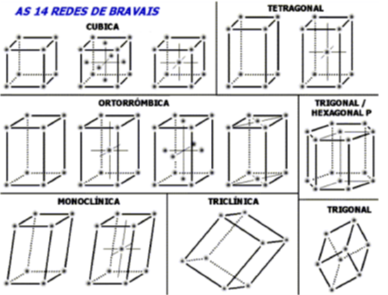
A Figura 3.12 mostra uma célula unitária cúbica, em que . Nela você pode evidenciar a divisão entre as faces, arestas e vértices entre os cubos. Para celas cúbicas, as abreviações são (cúbica simples), (cúbica de corpo centrado) e (cúbica de face centrada).
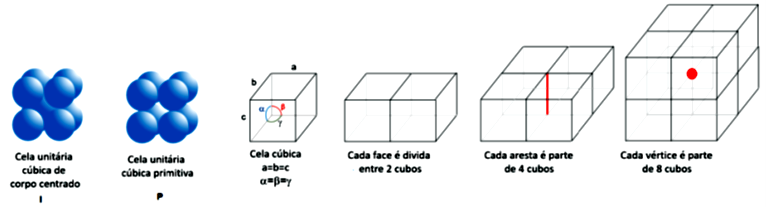
Esta análise permite identificar a quantidade de átomos em uma cela. Os átomos que estão no vértice são divididos entre oito celas, portanto, temos de átomo para cada vértice. Em uma cela cúbica simples ( de átomo por vértice, sendo oito vértices, no total teremos um átomo por cela. Os átomos que estão no centro em uma cela cúbica de corpo centrado () contam inteiramente para uma cela, somando aos átomo dos vértices, uma cela cúbica de corpo centrado tem dois átomos por cela. Já os átomos que estão em uma face são divididos entre duas celas, portanto, soma-se de átomos para cada cela. Com isso, numa cela cúbica de face centrada (), temos os átomos dos vértices e átomo multiplicado por seis faces do cubo, resultando em um átomo dos vértices e três átomos das faces, totalizando quatro átomos. Para uma cela com átomos centrados em duas faces você conta um átomo dos vértices e duas faces com átomo cada face, tendo mais um átomo, somando dois átomos no total. A massa total de uma cela será o número de átomos que a compõe, multiplicando a massa molar do elemento.
O empacotamento adotado pelos átomos garante que estes se organizem utilizando o menor espaço possível, entretanto, existem alguns espaços vazios, os buracos. É possível calcular a fração do espaço ocupado pelos átomos, chamado de fator de empacotamento atômico, na cela cúbica através do volume do cubo e do volume dos átomos.
4) Sólidos iônicos: compostos iônicos são constituídos por íons, conectados por interações eletrostáticas. Os sólidos iônicos são duros, quebradiços, com elevados pontos de fusão e, quando solúveis em água, são bons condutores elétricos. Assim como nos sólidos metálicos, os sólidos iônicos se organizam em retículos cristalinos, sendo a cela unitária a menor unidade organizacional repetida no sólido. A diferença entre os compostos iônicos e metálicos é que nos compostos iônicos dois átomos de tamanhos diferentes se organizam na cela.
O empacotamento do NaCl é chamado de sal-gema, e se assemelha a um arranjo cúbico de corpo centrado, porém expandido, evitando que íons de mesma carga se repilam. Já o cloreto de césio se compacta como uma cela cúbica de corpo centrado. Nos dois casos, a proporção entre os íons é 1:1, lembre-se de que os átomos do vértice são divididos entre oito celas, enquanto os das faces são divididos entre duas. Os dois arranjos estão descritos na Figura 3.13.
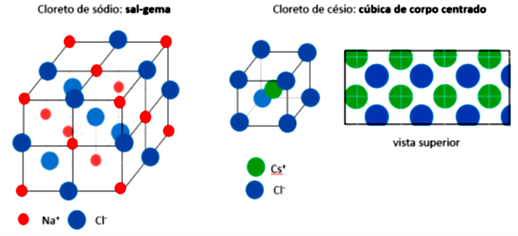
O número de coordenação para os compostos iônicos é calculado pela proporção de íons de sinal oposto que estão circulando um determinado íon. Para o sal-gema, o número de coordenação dos cátions é idêntico ao dos ânions, ou seja, seis, sendo descrito como tendo coordenação-(), em que o primeiro número corresponde à coordenação do cátion e o segundo à coordenação do ânion. Esta mesma estrutura você irá observar no , , e . Para o cloreto de césio, o número de coordenação é (). Para você determinar qual é o arranjo de cada composto iônico você deve calcular a razão radial ():
Quandoa estrutura provável é de sal-gema. Para um número maior de ânions se ajusta na volta do cátion, como o cloreto de césio que adota um arranjo cúbico de corpo centrado expandido. Para temos cátions muito menores que ânions, sendo um exemplo deste caso uma estrutura blenda de zinco (ou esfarelita), encontrada pela primeira vez para o , apresentando coordenação-(). Você deve ficar atento que embora seja um ótimo indicativo, existem muitas exceções.
A transformação do estado sólido para o estado líquido é denominada de fusão. Energia deve ser fornecida ao sistema para que as moléculas aumentem sua energia cinética e passem a líquidos, em que esta energia é absorvida como energia térmica na fusão e sua variação é a entalpia de fusão (). O processo inverso à fusão é a cristalização e sua energia corresponde a , ou seja, a energia é liberada no processo. O ponto de fusão corresponde à temperatura em que ocorre a passagem de um sólido para um líquido. Baixos pontos de fusão correspondem a entalpias de fusão menores, assim como pontos de fusão elevados indicam entalpias de fusão elevadas. O ponto de fusão de uma substância fornece diversas informações sobre ela. Sólidos cristalinos puros apresentam ponto de fusão bem definidos, sendo usualmente utilizado como dado de caracterização de um composto. Já sólidos amorfos fundem ao longo de uma faixa de temperatura, como é o caso do vidro. Lembre-se de que sólidos amorfos não apresentam organização molecular repetida.
Além de dados sobre a pureza, como no ponto de ebulição, a temperatura em que uma amostra funde revela dados sobre as forças intermoleculares. Compostos que se mantêm unidos por interações fortes, como os sólidos iônicos, apresentam pontos de fusão maiores que compostos moleculares (interações eletrostáticas são mais fortes que as forças de Van der Waals ou ligações de hidrogênio). À medida que ocorre o aumento da massa molecular em uma série de compostos, o ponto de fusão também aumenta, devido as forças de London serem mais fortes em moléculas maiores. Em sólidos iônicos, quanto menor o tamanho do íon ou maior sua carga, maior será a interação eletrostática, portanto, maior o ponto de fusão. Isso pode ser observado na série de sais (), (), () e (). Para os sólidos metálicos, alguns como o mercúrio (), são líquidos a temperatura ambiente, já outros como o tungstênio () são sólidos a temperaturas bem elevadas. Estas características definem muito suas aplicações.
Alguns compostos podem passar diretamente da fase sólida para a fase gasosa em um processo conhecido como sublimação, esta energia deve ser fornecida para o sistema ().
As condições de temperatura e pressão definem se um composto será sólido, líquido ou gasoso, e em algumas condições, mais de um estado pode coexistir. Podemos representar todas estas informações em um único gráfico chamado de diagrama de fases. A partir de um diagrama de fases você consegue obter informações sobre qual será o estado da matéria em diferentes temperaturas e pressões. Para a água, o diagrama de fases está descrito na Figura 3.14. As curvas , e demarcam o equilíbrio entre as fases. Note que a inclinação da reta é negativa e isso pode ser explicado pelo fato de o gelo apresentar maior volume que a água. A pressões maiores, a água apresenta uma maior tendência a ser líquida, pois ocupa menos volume que sólida, logo, precisamos de uma temperatura ligeiramente maior para realizar a fusão. Note que em combinações de pressão e temperatura que fiquem entre as linhas e , você terá água líquida (por exemplo pressão ambiente de e temperatura de ). Seguindo esta análise, o ponto a determina uma condição em que a água está na forma sólida. Ao aumentarmos a temperatura, mantendo a pressão constante, chegaremos até o ponto , em que há equilíbrio entre as fases sólida e líquida, seguindo o aumento da temperatura, chegamos a uma condição em que a água como um líquido até o ponto , no qual ocorre a passagem para a fase gasosa e, a partir deste ponto, em qualquer temperatura a água será um gás.
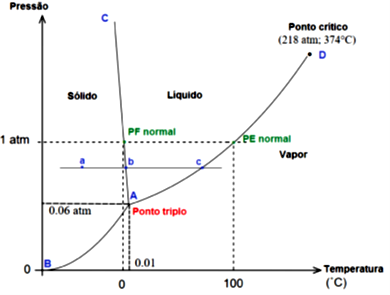
Neste diagrama, cabe ressaltar ainda que o ponto de fusão e ebulição normais (pressão ao nível do mar) são as temperaturas em que a água muda de fase (fusão e evaporação, respectivamente). O ponto triplo é aquele em que as três fases estão em equilíbrio e ponto crítico define que a partir dali, não há mais separação entre as fases líquida e vapor.
Vamos Exercitar?
Estudante, após compreender as características e propriedades dos compostos sólidos, conhecer a classificação deles em cristalinos e amorfos, as propriedades das estruturas sólidas cristalinas em sólidos reticulares, moleculares, iônica e metálica, as características de empacotamento, as células unitárias, tópicos fundamentais para o desenvolvimento da ciência e o desenvolvimento de materiais, você finalizou seu estudo com as definições de diagrama de fases.
Desse modo, vamos retomar o estudo dos novos materiais. Um dos caminhos para escolha de novos metais é consultar tabelas de densidade desses materiais, porém você pode resolver isso de uma maneira muito mais interessante. Você pode indicar um grupo de metais de acordo com seus empacotamentos. Para justificar sua resposta, pode calcular o fator de empacotamento atômico para cada tipo de empacotamento.
Para isso, deve dividir o volume da esfera pelo volume da cela unitária. Vamos realizar o cálculo para duas celas cúbicas, pois os metais mais interessantes para a pesquisa apresentam, ou arranjo cúbico de face centrada ou, cúbico de corpo centrado.
1) Para cela unitária cúbica de face centrada: nesta cela temos o total de quatro átomos e pelo teorema de Pitágoras sabemos que . Logo, o volume do cubo será dado por . O volume da esfera é , como temos quatro átomos, o volume será de . Com isso:
2) Para a cela unitária de corpo centrado: temos dois átomos (um do centro e um somando os vértices). A aresta deste cubo, como descrito, é dada por , sendo então o volume do cubo . O volume da esfera é multiplicado pelo número de átomos () e assim temos:
Com isso, você conclui que os metais com empacotamento cúbico de corpo centrado têm mais espaços vazios. São eles: ferro, cromo, vanádio, nióbio, tântalo, molibdênio, tungstênio. Você nem listou os elementos do grupo 1 e 2, pois sua elevada reatividade frente à água não permite que sejam utilizados nesta pesquisa. Além dessa solução, você pode pensar em pontos extras e adicionais sobre o problema apresentado. Continue estudando!
Saiba Mais
Para saber mais sobre as características dos compostos que se encontram em estado sólido, acesse a biblioteca virtual e faça a leitura do capítulo 11, Atrações intermoleculares e as propriedades dos líquidos e sólidos, do Livro: Química – A natureza molecular da matéria, v. 1, disponível na Minha Biblioteca.
JESPERSEN, Neil D.; HYSLOP, Alison. Química - A Natureza Molecular da Matéria - Vol. 1, 7ª edição. Rio de Janeiro: Grupo GEN, 2017. Disponível em: https://integrada.minhabiblioteca.com.br/#/books/9788521633969/. Acesso em: 03 mar. 2024.
Para compreender e aprofundar seus conhecimentos sobre a estrutura e as propriedades dos compostos em estado sólido, faça a leitura do artigo: “Estado Sólido na Indústria Farmacêutica: Uma breve revisão”, disponível em: http://dx.doi.org/10.5935/1984-6835.20150123. Acesso em: 03 mar. 2024.
Por fim, aprofunde seus conhecimentos sobre a estrutura dos sólidos iônicos por meio da leitura do texto: “Estrutura de sólidos iônicos”, disponível em: https://cesad.ufs.br/ORBI/public/uploadCatalago/11020317012017Quimica_Inorganica_I_aula_05.pdf. Acesso em: 03 mar. 2024.
Referências Bibliográficas
ATKINS, P.; JONES, L. Princípios de química: questionando a vida moderna e o meio ambiente. 5. ed. Porto Alegre: Bookman, 2009.
DREKENER, R. L. Química Geral. Londrina: Editora e Distribuidora S.A., 2017
KOTZ, J. C. et al. Química geral e reações químicas. 2. ed. São Paulo: Cengage Learning, 2014. v. 1.
Aula 4
Soluções e seu Comportamento
Soluções e seu Comportamento
Olá, estudante! Nesta videoaula você irá conhecer as características, propriedades e comportamento das soluções, sobre as propriedades coligativas e sobre os coloides. Esse conteúdo é importante para sua prática profissional, pois eles são aplicados na formulação de produtos, controle de qualidade, processos industriais, tecnologia de alimentos, ambiental, desenvolvimento de materiais e muito mais, garantindo eficiência e segurança em várias aplicações. Esteja pronto para embarcar nesta jornada de aprendizado! Vamos lá!!!
Ponto de Partida
Olá, estudante! Você já se perguntou por que uma pitada de sal faz a água ferver mais rápido? Ou por que alguns alimentos têm uma textura mais cremosa do que outros? Para compreender essas questões, explore o mundo das soluções, compreendendo o comportamento de soluções, as propriedades coligativas e o que vem a ser uma dispersão coloidal.
Nesta aula você conhecerá e compreenderá as características, propriedades e comportamento de soluções, assim como as características, propriedades e classificação de solutos e solventes. A partir da quantidade de soluto na solução, você será levada a trabalhar com as propriedades coligativas, que são fundamentais em diferentes processos industriais. Por fim, você vai explorar as características de partículas coloidais e como estas se comportam quando formam dispersões coloidais, apresentando diferentes tipos de aplicações.
Desse modo, para aplicar esse conteúdo, vamos pensar no abaixamento da pressão de vapor na indústria farmacêutica. Uma das formas de empregar esse conteúdo é por meio da produção de medicamentos por meio da técnica de liofilização, também conhecida como "secagem por congelamento". Nesse processo, o medicamento é congelado a uma temperatura muito baixa, o que reduz significativamente sua pressão de vapor. Em seguida, o gelo é removido por sublimação a vácuo, sem que ocorra a fusão, resultando na obtenção de um produto sólido e seco. Esse processo é especialmente útil para medicamentos sensíveis ao calor ou à umidade, pois preserva sua estabilidade química e biológica. Mas como podemos determinar o abaixamento da pressão de vapor de uma solução. Para isso, calcule a pressão de vapor de água, na temperatura de , em uma solução que foi preparada pela dissolução de de um não eletrólito, a sacarose, em de água. Prepare-se para uma jornada emocionante rumo ao entendimento de fenômenos químicos cruciais que ocorrem em soluções! Bons estudos!
Vamos Começar!
Estudante, quando respiramos, o ar atmosférico corresponde a uma mistura ou uma substância pura? Se o ar atmosférico é uma mistura, como ela é classificada? É possível que se obtenha uma solução do ar atmosférico? As soluções correspondem a uma mistura homogênea de duas ou mais substâncias, nas quais o solvente dissolve o soluto. Esta dinâmica entre substâncias, solvente e soluto, é encontrada na natureza e é replicada em laboratórios, onde desempenha um papel vital em processos industriais, em reações químicas e até mesmo na sobrevivência dos seres vivos. Mas por que precisamos conhecer e compreender as soluções, suas propriedades, características e, principalmente, seu comportamento?
Uma solução é uma mistura homogênea na qual um componente, chamado solvente (que se encontra em maior quantidade na solução), dissolve outra substância, chamada de soluto (que se encontra em menor quantidade na solução). A combinação resultante dessa mistura exibe propriedades uniformes em todo o volume, sem separação visível dos componentes, resultando em uma mistura homogênea. Embora podemos obter soluções a partir de diferentes solventes, a água é reconhecida como solvente universal, pois ela exerce um papel preponderante na formação de soluções, mas outros líquidos, gases e sólidos também podem desempenhar esse papel de solvente nas soluções.
As soluções podem ser classificadas com base no estado físico dos componentes: soluções sólidas, líquidas e gasosas. Além disso, as soluções podem ser classificadas de acordo com a quantidade de soluto dissolvido em relação ao solvente: soluções diluídas, concentradas e saturadas.
Uma solução sólida é formada quando diferentes substâncias se misturam de forma uniforme em estado sólido. É possível observar a formação desse tipo de solução em ligas metálicas, como na fabricação de aço, por exemplo, entre outros diferentes tipos de metal que são misturados para criar um material mais resistente. Essas soluções têm muitos usos na indústria, como na produção de materiais de construção e peças de máquinas. Já uma solução líquida é aquela que corresponde a uma mistura homogênea de duas ou mais substâncias, onde o solvente é um líquido. Na natureza temos muitas soluções líquidas disponíveis, onde a água (solvente) misturada com, por exemplo, um sal (soluto), forma uma solução líquida, como é o caso das águas dos mares e oceanos (desconsiderando a presença de partículas sólidas). Essas soluções são comuns em muitos aspectos da vida cotidiana, desde a preparação de alimentos e bebidas até processos industriais e produtos de limpeza. Além dessas, temos as soluções gasosas, elas correspondem a uma mistura homogênea de gases, onde o gás é o solvente e o soluto pode ser outro gás ou uma substância dispersa. Por exemplo, o ar atmosférico é uma solução gasosa composta principalmente de nitrogênio e oxigênio. Essas soluções são essenciais em processos industriais, como na produção de gases industriais e em aplicações em engenharia química.
Como uma solução é formada por soluto e solvente, temos que o solvente é a substância que dissolverá outra substância. Suas propriedades e classificação variam de acordo com a natureza química e física da substância. As propriedades dos solventes podem influenciar diretamente nas propriedades da solução, como a solubilidade, viscosidade, ponto de ebulição e condutividade elétrica. Os solventes podem ser classificados de diferentes maneiras, incluindo solventes polares e apolares, protônicos e aprotônicos.
Os solventes polares são aqueles cujas moléculas têm uma distribuição desigual de cargas elétricas, resultando em um dipolo elétrico permanente. Isso permite que solventes polares interajam bem com solutos polares, como íons e compostos iônicos, facilitando sua dissolução. A água, álcoois e acetona são exemplos de solventes polares. Por outro lado, os solventes apolares são aqueles cujas moléculas não possuem dipolos elétricos significativos. Eles interagem principalmente por forças de dispersão de London e são eficazes na dissolução de solutos apolares, como hidrocarbonetos e óleos. O benzeno, o hexano e o tetracloreto de carbono são exemplos de solventes apolares. Quanto aos solventes protônicos, eles são aqueles que possuem átomos de hidrogênio ligados diretamente a átomos de oxigênio, nitrogênio ou enxofre, que são bastante ácidos em relação ao próton. Esses solventes podem doar ou aceitar prótons quando participam de reações químicas. O ácido acético e a água são exemplos desse tipo de solvente. Já os solventes aprotônicos são aqueles que não possuem hidrogênios ligados a oxigênio, nitrogênio ou enxofre, e, portanto, não podem doar prótons. O éter dietílico, a acetona e o diclorometano são exemplos dessa classe de solventes, que são frequentemente utilizados em reações químicas onde a presença de prótons é indesejável.
Quanto ao soluto, ele é a substância que é dissolvida em um solvente para formar uma solução. Suas propriedades e classificação dependem da natureza química e física da substância. As propriedades dos solutos podem afetar as propriedades da solução, como o ponto de fusão, ponto de ebulição, pressão de vapor e condutividade elétrica. Os solutos podem ser classificados de várias maneiras, incluindo solutos iônicos, moleculares e coloidais, dependendo da forma como se dissolvem e interagem com o solvente.
A presença do soluto também altera as propriedades físicas do solvente, dando origem às propriedades coligativas. Estas são características são dependentes apenas do número de partículas do soluto, como o abaixamento da pressão de vapor, o aumento do ponto de ebulição, a diminuição do ponto de congelamento e a pressão osmótica. Essas propriedades têm diversas aplicações práticas, como em processos industriais, farmacêuticos e alimentícios.
Siga em Frente...
Propriedades Coligativas
As propriedades coligativas são as características físicas de uma solução que dependem exclusivamente da quantidade de partículas de soluto dissolvidas em um determinado volume de solvente, independentemente de sua natureza química. Essas propriedades incluem o abaixamento da pressão de vapor, o aumento do ponto de ebulição, a diminuição do ponto de congelamento e a pressão osmótica. Essas propriedades são características físicas das soluções e estão intimamente relacionadas às interações entre as moléculas do solvente e do soluto na solução.
Desse modo, as soluções e as propriedades coligativas estão intrinsecamente ligadas, pois as mudanças nas propriedades das soluções são consequência direta da presença de soluto na solução. Essas propriedades têm amplas aplicações em diversas áreas, desde a indústria alimentícia e farmacêutica até a pesquisa científica e a produção de materiais industriais.
Agora você vai conhecer e compreender cada uma dessas propriedades.
Abaixamento da Pressão de Vapor: ocorre quando um soluto é adicionado a um solvente para formar uma solução, resultando na redução do número de partículas de solvente na superfície. Isso diminui a taxa de evaporação do solvente, resultando em um abaixamento da pressão de vapor em relação à do solvente puro.
Essa propriedade é utilizada em diferentes áreas, como na indústria farmacêutica, sendo que na produção de medicamentos, o abaixamento da pressão de vapor é fundamental para o preparo de soluções, suspensões e emulsões farmacêuticas. Na indústria química, ela é aplicada, por exemplo, na produção de solventes e produtos químicos, sendo o conhecimento do abaixamento da pressão de vapor essencial para o controle de processos de destilação e evaporação.
Aumento do Ponto de Ebulição: essa propriedade ocorre devido à presença do soluto, que reduz a taxa de evaporação do solvente e, consequentemente, aumenta a pressão de vapor da solução. Esse processo resulta em uma demanda de temperatura mais alta para que a pressão de vapor da solução se iguale à pressão atmosférica.
Essa propriedade pode ser aplicada na indústria petroquímica, onde temos o refinamento do petróleo. O aumento do ponto de ebulição, nesse processo, é utilizado para separar diferentes componentes do petróleo por meio da técnica de destilação fracionada. Já em laboratórios de pesquisa, como os laboratórios químicos, o aumento do ponto de ebulição é empregado para purificar substâncias e separar misturas por destilação.
Diminuição do Ponto de Congelamento: ocorre quando um soluto é adicionado a um solvente, resultando na redução do ponto de congelamento da solução em relação ao do solvente puro. Isso ocorre porque o soluto interfere nas interações entre as moléculas de solvente, dificultando a formação de estruturas cristalinas sólidas. Essa propriedade é aplicada, por exemplo, na indústria alimentícia, na produção de sorvetes e alimentos congelados, onde a diminuição do ponto de congelamento é fundamental para controlar a textura e o tempo de solidificação dos produtos. Também é possível aplicar essa propriedade na indústria automotiva, pois na fabricação de fluidos anticongelantes para veículos, a diminuição do ponto de congelamento é essencial para evitar danos causados pelo congelamento de líquidos em sistemas de refrigeração.
Pressão Osmótica: é a pressão necessária para impedir o movimento líquido através de uma membrana semipermeável, que separa uma solução de um solvente puro. Essa propriedade é diretamente proporcional à concentração de partículas de soluto na solução. Essa propriedade apresenta aplicações como na biologia, onde na fisiologia celular, a pressão osmótica é fundamental para a regulação do equilíbrio osmótico entre as células e seu ambiente. Na indústria alimentícia, a propriedade encontra emprego, por exemplo, na produção de alimentos enlatados e conservas, onde a pressão osmótica é utilizada para preservar os alimentos e prolongar sua vida útil.
Assim temos que as propriedades coligativas estão diretamente relacionadas as comportamento de soluções e desempenham um papel fundamental em uma ampla gama de aplicações industriais, farmacêuticas, alimentícias, químicas e biológicas, sendo sua compreensão fundamental, pois permite o desenvolvimento de processos mais eficientes.
Coloides e dispersões coloidais
Soluções correspondem a uma mistura homogênea formada entre um solvente e um soluto, porém, em diferentes situações, podemos encontrar partículas sólidas dispersas em um meio líquido, originando uma mistura heterogênea. Para compreender esse tipo de mistura, começamos com a definição de coloides.
Os coloides são sistemas em que partículas de uma substância, denominadas fase dispersa, estão dispersas de maneira uniforme em outra substância, chamada de meio dispersante. A característica distintiva dos coloides é o tamanho das partículas dispersas, que estão na faixa de a nanômetros (), tornando-os intermediários entre as soluções verdadeiras (com partículas menores que ) e as suspensões (com partículas maiores que ).
As dispersões coloidais correspondem a um tipo de coloide em que partículas sólidas ou líquidas estão dispersas em um meio líquido. As partículas coloidais são grandes o suficiente para dispersar a luz e criar um efeito Tyndall, visível quando um feixe de luz é projetado através do coloide. Essas partículas são mantidas dispersas pela agitação térmica, impedindo que se separem e sedimentem ao longo do tempo.
Existem diferentes tipos de coloides, dependendo da natureza das partículas dispersas e do meio dispersante. Os coloides podem ser classificados em sols, géis e emulsões, com base em suas propriedades físicas e químicas. Os sols são coloides em que a fase dispersa é líquida e a fase dispersante é líquida ou sólida. Eles podem ser estáveis ou instáveis, dependendo da interação entre as partículas dispersas e o meio dispersante. Os géis são coloides em que a fase dispersa é sólida e a fase dispersante é líquida. Eles têm uma estrutura semelhante a uma esponja e podem ser usados em uma variedade de aplicações, desde produtos alimentícios até produtos farmacêuticos e cosméticos. Já as emulsões são coloides em que a fase dispersa é líquida e a fase dispersante é líquida. Elas são amplamente utilizadas na indústria alimentícia, cosmética e farmacêutica devido à sua capacidade de combinar ingredientes que normalmente não se misturam.
As propriedades dos coloides, como viscosidade, estabilidade e capacidade de dispersão de luz, são influenciadas pelo tamanho, forma e carga das partículas dispersas, bem como pela natureza do meio dispersante. A estabilidade dessas partículas pode ser afetada por vários fatores, como pH, concentração de sais e temperatura. Mudanças nas condições ambientais podem levar à coagulação ou floculação das partículas dispersas, resultando na separação do coloide em fases distintas, para evitar a ocorrência desse problema, são adicionados estabilizantes ou agentes dispersantes para manter as partículas dispersas uniformemente distribuídas no meio dispersante.
Vamos Exercitar?
Estudante, após conhecer e compreender as soluções e as dispersões coloidais, entender as propriedades e classificações do soluto e solvente, e a partir da quantidade de soluto, trabalhar com as propriedades coligativas. Chegou a hora de aplicar o conteúdo na determinação do abaixamento da pressão de vapor de uma solução, sendo está uma propriedade coligativa.
Para solucionar a questão, precisamos aplicar a Lei de Raoult, que nos diz:
Onde é a pressão de vapor do solvente puro e corresponde a fração molar do solvente e a pressão de vapor do solvente na solução.
Nesta aplicação, é esperado uma pressão de vapor mais baixa na presença do soluto. Desse modo, é determinada a pressão de vapor do solvente na solução (ATKINS; JONES, 2009)
Assim temos:
A partir dessa informação, é determinado o número de mols de cada espécie.
A fração molar da água corresponde a:
Para encontrar a pressão do solvente na solução, precisamos do valor da pressão do solvente puro. De acordo com Atkins e Jones (2009), a pressão do solvente puro, . Agora é determinado o abaixamento da pressão da solução:
Além dessa solução, você pode pensar em pontos extras e adicionais sobre o problema apresentado. Continue estudando!
Saiba Mais
Para saber mais sobre as soluções, suas propriedades, características e comportamento, acesse a biblioteca virtual e faça a leitura do capítulo 12, Propriedades físicas das soluções, do livro “Química”, disponível na Minha Biblioteca.
CHANG, Raymond; GOLDSBY, Kenneth A. Química. Porto Alegre: Grupo A, 2013. Disponível em: https://integrada.minhabiblioteca.com.br/#/books/9788580552560/. Acesso em: 03 mar. 2024.
Para compreender e aprofundar seus conhecimentos sobre as propriedades coligativas, faça a leitura do texto: “Propriedades coligativas”, disponível em: https://cesad.ufs.br/ORBI/public/uploadCatalago/16292008042013Fisico-Quimica_II_Aula_4.pdf. Acesso em: 03 mar. 2024.
Por fim, aprofunde seus conhecimentos sobre as dispersões coloidais, por meio da leitura do artigo “O mundo dos coloides”, disponível em: https://edisciplinas.usp.br/pluginfile.php/6718560/mod_resource/content/2/Mundo_coloides.pdf. Acesso em: 03 mar. 2024.
Referências Bibliográficas
ATKINS, P.; JONES, L. Princípios de química: questionando a vida moderna e o meio ambiente. 5. ed. Porto Alegre: Bookman, 2009.
Encerramento da Unidade
Propriedades dos Estados Físicos da Matéria
Videoaula de Encerramento
Olá, estudante! Nesta videoaula você irá rever os conceitos pertinentes aos diferentes estados físicos da matéria, sólidos, líquidos e gases e por fim, compreender o comportamento de soluções. Esse conteúdo é importante para a sua prática profissional, pois é essencial para desenvolver produtos inovadores, otimizar processos industriais e garantir a segurança e eficácia de produtos farmacêuticos, alimentos e materiais em diversas áreas da prática profissional. Bons estudos! Vamos lá!
Ponto de Chegada
Olá, estudante! Para desenvolver a competência desta Unidade, que é conhecer o comportamento da matéria que se encontra em diferentes estados físicos, sólido, líquido e gasoso, você precisa compreender inicialmente como é caracterizada a matéria em seus estados físicos, no estado gasosa a matéria não possui forma e nem volume definido, no estado líquido, a matéria possui volume definido, porém, não possui forma definida, já no estado sólido, a matéria apresenta forma e volume definido. Após compreende a constituição da matéria nos diferentes estados físicos, você precisa trabalhar com as propriedades e características de cada estado físico. No estado gasoso, temos a propriedade de expansão e compressibilidade, e uma característica importante desse estado é compreender a variação da pressão do sistema, desse modo, realizamos relação entre temperatura, pressão e volume por meio das Lei dos Gases. Para facilitar os cálculos, consideramos os gases como ideais, e a partir disso, temos a Lei dos Gases Ideais, que é aplicada a diferentes situações. Outra Lei importante é a Lei das pressões parciais de Dalton, que nos diz que a pressão total do sistema é igual a soma da pressão parcial dos gases que o compõe. Mas é preciso observar que em algumas situações, os gases podem sofrer desvios em relação a essas leis, como em situação em que a pressão é muito elevada.
Ao se trabalhar com os líquidos, você precisa compreender as propriedades deles, por isso, incialmente, é importante compreender características que envolvem o movimento das moléculas. Quanto as propriedades dos líquidos, temos várias, entre elas, podemos destacar a capilaridade e a tensão superficial, que são propriedades que grande aplicabilidade em várias áreas do conhecimento. Outro ponto importante dos líquidos é trabalhar com as forças intermoleculares, que são as forças existentes entre moléculas que afetam propriedades das substâncias. Entre elas temos a ligação covalente polar, a ligação de hidrogênio, a interação dipolo-dipolo, a interação dipolo-dipolo induzido e a dispersão de London.
Quanto aos sólidos, estes apresentam estruturas rígidas e, podem apresentar arranjo ordenado de seus átomos, partículas, íons ou moléculas em uma estrutura cristalina ou um arranjo desordenado em uma estrutura amorfa. Quando apresentam estrutura cristalina, os sólidos se apresentam como moleculares, reticulares, iônicos e metálicos. As estruturas nesse estado físico se repetem de acordo com um arranjo definido, que é determinado pela célula unitária. As células unitárias possuem 7 estruturas definidas, e a partir delas, podemos obter 14 estruturas, conhecidas como estruturas de Bravais, que corresponde ao arranjo tridimensional de pontos que descreve a repetição do retículo cristalino em sólidos. Ao conhecer os diferentes estados físicos da matéria, temos que observar os processos envolvidos nas mudanças de fases por meio do estudo dos diagramas de fases.
Por fim, você precisa conhecer as características de soluções e dispersão colidais. As soluções são amplamente empregadas em diferentes processos industriais e são constituídas de solvente e soluto, podendo cada um possuir diferentes classificações. Quando a quantidade de soluto na solução, podemos observar que podem ocorrer algumas alterações nas propriedades dos solventes, essas propriedades são conhecidas como Propriedades Coligativas e são amplamente aplicadas para obtenção de produtos do dia a dia, como os medicamentos.
Compreender os estados físicos da matéria e as soluções é fundamental para desvendar os segredos do universo ao nosso redor. Ao mergulhar nesse estudo, você terá a oportunidade de explorar as interações entre átomos e moléculas, desvendando os mistérios por trás das propriedades e comportamentos da matéria. Essa jornada não apenas ampliará seu conhecimento científico, mas também abrirá portas para uma série de aplicações práticas em diversos campos, desde a indústria até a medicina. Então, vamos embarcar nessa fascinante jornada do conhecimento! Bons estudos!
É Hora de Praticar!
Estudante, você é o responsável pelo processo de obtenção do pentacarbonilo de ferro () em uma indústria de insumos químicos. Este composto é utilizado em diversas outras indústrias como fonte de ferro carbonil, que é uma fonte bastante pura de ferro, utilizada, por exemplo, na indústria alimentícia (DAMODARAN et. al., 2010). Sua tarefa é analisar todo o processo e os fatores que devem ser levados em consideração. A reação para formação do pentacarbonilo de ferro, descrita a seguir, ocorre à elevada pressão e a .
Qual a quantidade de utilizada para produzir o composto desejado? Qual o tamanho do reator que deve ser adquirido para o processo? O que você deve levar em conta nesta escolha? Quais as interações presentes no líquido obtido como produto? Como se encontra o ferro sólido utilizado no processo? Pensando na situação proposta, reflita e responda aos seguintes questionamentos.
1) Pesquisando sobre o processo de obtenção do pentacarbonilo de ferro, encontrou que esta reação ocorre a , o que fez você e seu gestor decidirem implementar uma escala laboratorial do processo, a fim de testar o comportamento do sistema. Seu gestor pediu que você dimensionasse a equação, trabalhando com a massa dos reagentes, a fim de escolher o reator para o processo, isso pensando em inicialmente trabalhar com de ferro metálico. Qual a escala que será utilizada? Qual a pressão no reator com o uso da quantidade necessária de gás? Ela é suficiente para que a reação aconteça?
2) Após dimensionar o processo, agora, sua tarefa é pensar sobre o produto obtido. Você utiliza um sólido e um gás para obter um produto líquido. Como você retira o líquido do reator? Só escoar o líquido irá funcionar ou precisa de um solvente? Se utilizar um solvente, qual devem ser as características deste solvente para que você consiga remover o líquido totalmente do reator?
3) Ao realizar o procedimento, você observou um rendimento muito baixo do esperado e após revisar todos os passos não conseguiu pensar em outro problema senão a qualidade de um dos reagentes: o ferro. Seu gestor pediu que realizasse uma análise simples na matéria--prima que fosse capaz de determinar que o ferro utilizado estava puro. Como você pode fazer isso de uma forma rápida e simples? O ferro é um sólido metálico, como tal, ele se organiza de uma maneira bem definida. Bons estudos!
Reflita
Durante a fabricação de um medicamento líquido, é necessário entender como as forças intermoleculares influenciam a solubilidade dos componentes sólidos no solvente líquido. Como essas forças afetam a dissolução de um sólido no líquido e como essa compreensão pode ser aplicada para otimizar o processo de fabricação?
Um engenheiro precisa projetar um tanque de armazenamento para um gás inflamável. Como as propriedades dos gases, como compressibilidade e expansibilidade, afetam o design e a segurança do tanque? Como a compreensão das propriedades físicas dos gases pode influenciar a seleção do material do tanque e a forma como ele será utilizado e operado?
Um laboratório farmacêutico está desenvolvendo uma nova formulação de medicamento líquido que precisa ser administrado por via intravenosa. Como as propriedades coligativas, como o abaixamento do ponto de congelamento e o aumento do ponto de ebulição, podem ser aplicadas para controlar a osmolaridade da solução e garantir a segurança e eficácia do medicamento durante a administração intravenosa?
Resolução do estudo de caso
Como responsável técnico pela implementação da obtenção industrial de pentacabronilo de ferro, você começou a trabalhar com o dimensionamento da reação. Independentemente da escala, o produto de interesse é obtido pela reação:
Entretanto, como a reação ocorre a , você e seu gestor optaram por estudar o processo em escala piloto. Desenvolvendo o processo de obtenção de pentacarbonilo de ferro, você precisa inicialmente dimensionar a reação, trabalhando com a estequiometria dos reagentes, levando em consideração a utilização de de ferro metálico. Como este é um processo completamente novo para a indústria em que está trabalhando e não é desenvolvido por muitas outras, você e seu gestor decidiram implementar uma escala laboratorial.
Pensando em evitar a compra de um novo equipamento, foi decidido pelo uso de um reator ocioso no laboratório de escala piloto com capacidade de . Independentemente da escala, o produto de interesse é obtido pela reação:
Utilizando de ferro sólido, qual a quantidade de que deve ser utilizada? Isso corresponde a quantos ? Qual a pressão à temperatura ambiente? E qual a pressão na temperatura de , que é quando a reação ocorre? Esta pressão está de acordo com as condições reacionais?
Você precisa iniciar calculando quantos mols de ferro estão sendo utilizados. A massa molar do ferro é de . Para calcular quantos mols de ferro estão em , você deve realizar uma regra de 3:
Portanto, utilizando o coeficiente estequiométrico que indica que de ferro reage com de , precisamos de de .
Como nas corresponde a , esta quantidade corresponde a de gás nas , porém, o volume do reator é de .
Para sabermos qual a pressão deste gás neste volume, devemos utilizar , isolando , teremos .
À temperatura ambiente (), teremos:
Na temperatura da reação (), teremos:
Você precisa lembrar que a reação, sem catalisadores, ocorre a uma pressão de . Sabendo que corresponde a , teremos, portanto, e , ou seja, tratando o CO como um gás ideal, em nenhuma das temperaturas (ambiente ou ), a pressão necessária para a reação ocorrer é atingida. Utilizando a lei de Boyle, podemos chegar no volume próximo que o reator deve ter para atingir a pressão necessária: , portanto, , sendo. Se o reator possuir volume ajustável, pode ser utilizado, caso não, você pode sugerir um reator de com menos mols de , porém, não utilizaria o reator ocioso. Outra opção é utilizar o reagente em excesso.
Para calcular o número de mols necessários para atingir a pressão de , você novamente utiliza a lei dos gases ideais, lembrando de passar para :
de reagem (em excesso) com de , que corresponde à massa de .
Agora, vamos pensar em como retirar o líquido do reator. Você inicia a resolução do problema estudando as propriedades do pentacarbonilo de ferro. Seu ponto de ebulição é , isso já sinaliza que, inicialmente, deve diminuir a temperatura do reator e então diminuir a pressão, pois se você diminui a pressão a altas temperaturas (), ele será um gás e será perdido. O ponto de fusão do produto é de , portanto, temperaturas muito baixas e altas pressões podem torná-lo sólido. Como um dos reagentes é sólido e o outro é gasoso, a melhor maneira de obter o composto é mesmo como um líquido.
Quanto mais próximo a , mais viscoso o líquido será e mais difícil será escoá-lo do reator. Você aprendeu nesta seção que a temperatura está relacionada com a viscosidade, sendo que quanto maior a temperatura, menor a viscosidade.
Esta molécula não é polar, sendo caracterizada por ser um composto de coordenação, em que o ferro se encontra coordenado com e não covalentemente ligado. Esta molécula, por esta característica, é apolar, portanto, o uso de solventes polares não auxilia na remoção do composto que permanecer aderido ao reator por forças de coesão.
O melhor é utilizar solventes apolares como o éter etílico, que possui a vantagem de ter um baixo ponto de ebulição (), podendo ser facilmente removido do produto por evaporação. Note que o uso de solvente pode ser aplicado na planta piloto, porém, na indústria, o uso de éter é desaconselhado devido a seu grande potencial em causar acidentes (explosões).
Uma técnica bastante utilizada para remoção de solventes consiste em utilizar um equipamento chamado rota-evaporador que reduz a pressão do sistema para que a evaporação ocorra mais facilmente. O princípio deste equipamento é que, ao diminuirmos a pressão do sistema, a pressão de vapor se iguala a esta pressão a uma temperatura mais baixa que se estivéssemos a pressão atmosférica. Com isso, é necessário menor aquecimento. Outra opção é a utilização de destilação como processo de purificação para grandes quantidades, e este processo é baseado na diferença dos pontos de ebulição.
Para seu processo, baseado nas características do produto, você propõe, então, que a temperatura diminua antes da pressão e que o líquido seja escoado, por exemplo, à temperatura ambiente. Se as forças de adesão forem intensas, você pode propor um aumento da temperatura ou, para a planta piloto, a utilização de um solvente, sendo que o solvente pode ser removido utilizando evaporação ou destilação.
Por fim, você realizou um teste em escala piloto, agindo de maneira bastante prudente. Após analisar a reação e o processo, não identificou nenhum erro que pudesse ser responsável pelo problema de rendimento. Além de encaminhar as amostras para o laboratório, seu gestor pediu que você pensasse em uma maneira simples e eficiente de indicar se o ferro estava puro ou não. Enquanto você encaminhava as amostras ao laboratório de análise, começou a pensar o que mais poderia ser feito, assim poderia contornar o problema com nova matéria-prima.
A densidade é uma propriedade intrínseca da matéria, ou seja, independe do tamanho da amostra, e pode ser calculada a partir de dados do tipo de empacotamento do metal. O ferro apresenta arranjo cúbico de corpo centrado. Para um cubo, deve lembrar que o volume é dado por
, sendo que para este empacotamento deve usar como guia a diagonal do corpo da cela (), pois é onde os átomos se tocam. Para encontrar a aresta, você deve utilizar o teorema de Pitágoras () que também diz que e, portanto, . Sabemos, então, que , sendo .
Para encontrarmos a massa, devemos verificar a massa molar do ferro, que é . Este arranjo encerra dois átomos, então, teremos a densidade () dada por:
O raio do ferro é (). Dessa forma, você terá a densidade dada por:
Esta é uma aproximação para a densidade. Agora faz-se necessário determinar a densidade de uma amostra de ferro que foi utilizada em sua reação. Este procedimento é simples, você deve unicamente utilizar um recipiente graduado, como uma proveta, por exemplo, pesar uma amostra de ferro e colocá-la na proveta com água, a variação do volume da água corresponde ao volume do objeto. Como você teve a massa pesada no início do processo você consegue calcular a densidade da amostra.
Você selecionou uma amostra de e verificou que o volume desta amostra é de . Com isso, a densidade de sua amostra será de:
Um valor bem diferente do esperado, você criou um alerta sobre a qualidade desta matéria-prima. Enquanto aguardava a confirmação do laboratório, foi ao estoque e pesquisou se havia outro lote de ferro metálico. Você, então, pôde repetir o processo e obter a reação em um rendimento bem melhor que o anterior, sendo necessário apenas pequenos ajustes. Após o resultado da reação, a análise laboratorial chegou, confirmando suas suspeitas de contaminação. Seu gestor ficou bastante satisfeito com sua pró atividade e conhecimentos básicos.
Dê o play!
Assimile
Estudante, está pronto para explorar um mundo fascinante de substâncias e suas propriedades? Convido você a embarcar em uma jornada de descoberta sobre os gases, líquidos, sólidos e soluções. Vamos começar falando sobre os gases, que são tão abundantes e importantes em nosso dia a dia. Vamos explorar a Lei dos Gases, que descreve como eles se comportam em diferentes condições de temperatura e pressão, e entender o conceito de gases ideais. Descobriremos também suas propriedades e características únicas, que influenciam desde a atmosfera terrestre até processos industriais.
Em seguida, mergulharemos nos líquidos, explorando fenômenos fascinantes como capilaridade, tensão superficial e as forças intermoleculares que governam seu comportamento. Não podemos esquecer dos sólidos, com sua estrutura cristalina ou amorfa, e seus arranjos ordenados que os tornam tão diversos e interessantes. Vamos investigar os diferentes tipos de sólidos e entender como eles se comportam em diferentes condições, explorando, no final, o diagrama de fases que revela suas transformações.
Por fim, você vai explorar o mundo das soluções, onde soluto e solvente vão originar uma mistura homogênea com as mais diversas aplicações. Você vai descobrir como as propriedades coligativas afetam o comportamento das soluções e explorar os características e propriedades dos coloides e das dispersões coloidais.
Prepare-se para conhecer e compreender o mundo da matéria e suas transformações. Bons estudos!
Referências
ATKINS, P.; Jones, L. Princípios de química - questionando a vida moderna e o meio ambiente. 5. ed. Porto Alegre: Bookman, 2009.
BARREIRO, E. J.; FRAGA, C. A. M. Química medicinal: as bases moleculares da ação dos fármacos. 2. ed. Porto Alegre: Artmed; 2008.
DAMODARAN, S.; PARKIN, K. L.; FENNEMA, O. R. Química de Alimentos de Fennema. 4. ed. 2010.
DREKENER, R. L. Química Geral. Londrina: Editora e Distribuidora S.A., 2017
KOTZ, J. C. et al. Química geral e reações químicas. 2. ed. São Paulo: Cengage Learning, 2014. v. 1.
RUSSEL, John B. Química geral. v. 2, 2. ed. São Paulo: Pearson Education do Brasil, 2011.